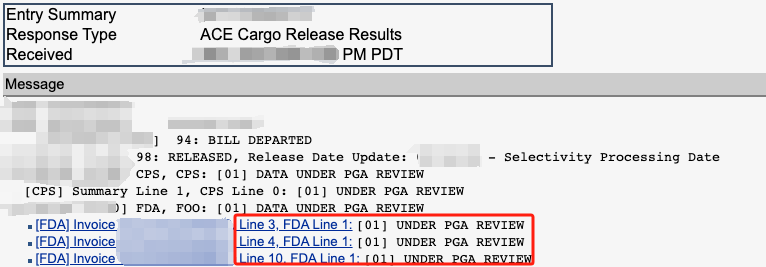
FDA 监管多种产品,包括食品、发射辐射的电子产品、医疗器械、烟草制品和化妆品等,每种受 FDA 监管的产品都受特定法规要求的约束,FDA 决定产品是否允许进入美国市场,并可拒绝任何违反或似乎违反《联邦食品、药品和化妆品法案》(FD&C Act)(Federal Food, Drug, and Cosmetic Act)规定的产品入境。
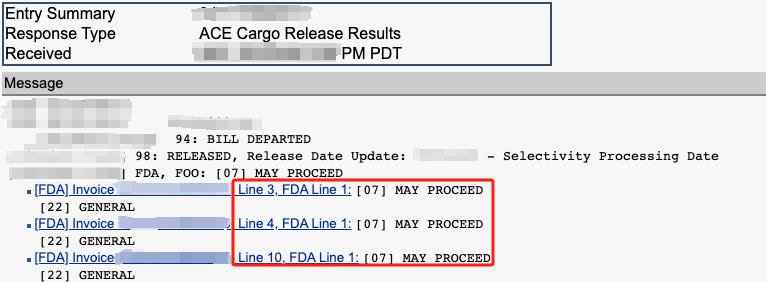
报关 Entry 处理流程(Entry process)始于 FDA 对申报 Entry 所需数据的筛查(Screening)。FDA 完成对所需数据筛查后,将继续进行进口处置程序(Import Disposition),并确定行动通知 NOA(Notice of action)。行动通知类型包括放行产品(Release the product)、要求提供补充信息(Request additional information)、要求提供样品进行评估(Request a sample for evaluation)或要求扣留入境产品(Request detention of the entry)。FDA 生成(Generates)进口处置决定(Import disposition)确定行动通知后,将向美国海关 CBP 及海关备案进口商 IOR(Importer of Record)发出通知,CBP 会根据需要将信息发送给报关行和其他相关方。

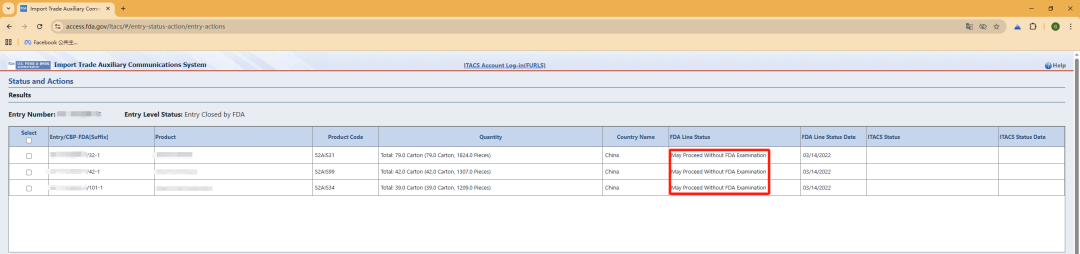
亦可使用 ITACS 系统查询 FDA 申报 Entry 的状态,
在 FDA 发出要求提供补充信息的行动通知后,若进口商未能提供所要求的信息可能导致 FDA 发出扣留(Detention)行动通知或 FDA 采取其他适当行动。
当 FDA 对受监管的某批进口货物进行检查后发现其不符合相关监管规定,则相关产品可能会被拒绝进入美国,拒绝入境(Import Refusals)的原因包括但不限于以下情况:
掺假(Adulterated),指产品受到污染、不安全或不符合适用标准; 误标(Misbranded,),指标签包含虚假或误导性信息; 未经批准的新药; -
禁止或限制销售。
以上列表并非 FDA 监管产品被拒绝入境的全部原因。如需了解具体被拒产品的信息,可以查看 FDA 进口拒绝报告 IRR,


文章为作者独立观点,不代表DLZ123立场。如有侵权,请联系我们。( 版权为作者所有,如需转载,请联系作者 )

网站运营至今,离不开小伙伴们的支持。 为了给小伙伴们提供一个互相交流的平台和资源的对接,特地开通了独立站交流群。
群里有不少运营大神,不时会分享一些运营技巧,更有一些资源收藏爱好者不时分享一些优质的学习资料。
现在可以扫码进群,备注【加群】。 ( 群完全免费,不广告不卖课!)







发表评论 取消回复